Tóm tắt (Abstracts)
Giới thiệu:Sốt rét hiện vẫn là vấn đề y tế công cộng tại các vùng nhiệt đới và cận nhiệt đới, đặc biệt tại khu vực Đông Nam Á và cận sa mạc Sahara, châu Phi. Việc đưa vào sử dụng artemisinine giúp ngăn chặn chủng ký sinh trùng Plasmodium falciparum đa kháng với các thuốc sốt rét cổ điển. Song gần đây, Tổ chức Y tế thế giới cảnh báo về khả năng kháng với artemisinin lan rộng sang các các quốc gia trong tiểu vùng sông Mê Kông sau khi xác định kháng thuốc này tại biên giới Thái Lan - Campuchia. Tại khu vực miền Trung Tây Nguyên, Việt Nam, thời điểm 2005-2010, một số thử nghiệm in vivo và điều tra hiệu quả tại các tuyến điều trị cho thấy thuốc giảm nhạy (WHO, 2011; Huỳnh Hồng Quang và cs., 2011). Sự xuất hiện và lan rộng kháng thuốc sốt rét, đặc biệt do chủng P. falciparum nguy hiểm có thể đe dọa nghiêm trọng đến thành quả phòng chống sốt rét Việt Nam.
Mục tiêu: Nghiên cứu tiến hành nhằm đánh giá hiệu lực thuốc phối hợp có gốc artemisinin trong điều trị sốt rét do P. falciparum chưa biến chứng.
Phương pháp:với thiết kế thử nghiệm lâm sàng không ngẫu nhiên, đánh giá hiệu quả theo phân loại của WHO gồm đáp ứng lâm sàng và ký sinh trùng đầy đủ (ACPR), thất bại điều trị sớm (ETF), thất bại lâm sàng muộn (LCF), thất bại ký sinh trùng muộn (LPF) và tỷ lệ ký sinh trùng dương tính ngày D3 như một chỉ điểm kháng thuốc.
Kết quả:Nghiên cứu tiến hành theo đề cương chuẩn của WHO, kết quả cho thấy tỷ lệ chữa khỏi (ACPR) của thuốc dihydroartemisinine plus piperaquine là 94.8%, đặc biệt có thất bại điều trị sớm (ETF) là 3.4% và thất bại lâm sàng muộn (LCF) là 1.7%, cùng với tỷ lệ tồn tại ký sinh trùng ngày D3 là 17% như một chỉ điểm nguy cơ kháng thuốc cao. 3 trường hợp LCF sau hiệu chỉnh PCR là tái nhiễm và tái phát.
Kết luận:Hiệu lực thuốc dihydroartemisinine plus piperaquine rất cao, lý tưởng cho điều trị sốt rét do P. falciparum, nhưng tỷ lệ ký sinh trùng D3 dương tính cao > 10% như một chỉ điểm và bằng chứng kháng đầu tiên xuất hiện tại cao nguyên Việt Nam. Phác đồ thuốc này cần phải giám sát hiệu lực để có thay đổi chính sách thuốc tốt hơn.
Từ khóa: Plasmodium falciparum, kháng thuốc artemisinin, hiệu lực
Giới thiệu
Sốt rét, “Vua của các bệnh” vẫn là bệnh truyền nhiễm quan trọng tiếp tục đe dọa đến nhân loại. Hơn 1 thế kỷ qua sau khi xác định tác nhân và hơn ½ thể kỷ tìm ra thuốc điều trị và hóa chất diệt côn trùng, bệnh được coi là cũ song cũng ảnh hưởng đến hơn 500 triệu người và hơn 3 triệuca tử vong mỗi năm. Thành công của Chương trình quốc gia Phòng chống sốt rét Việt Nam không thể không kể đến sự đóng góp quan trọng của các thuốc có hiệu lực cao, nhất là artemisinins và dẫn suất. Sự xuất hiện và lan rộng Plasmodium falciparum kháng với các thuốc cổ điển như chloroquin, sulphadoxine/pyrimethamine và mefloquine đã đưa ra những thách thức lớn trong phòng chống sốt rét tại khu vực châu Phi và Đông Nam Á. Đối mặt với sự gia tăng kháng thuốc, Tổ chức Y tế thế giới và Việt Nam đã khuyến cáo sử dụng thuốc phối hợp có gốc artemisinins (ACTs_artemisinin combination therapies) như ưu tiên trong điều trị tại Việt Nam. Các dẫn suất của artemisinins có tác động quan trọng về mặt lâm sàng trên điều trị sốt rét (SR) do P. falciparum đa kháng thuốc. Tuy nhiên, kinh nghiệm cho thấy kháng thuốc sẽ dẫn đến rút ngắn tuổi thọ của thuốc, nếu không áp dụng các biện pháp ngăn chặn kháng thì việc đầu tư phát triển thuốc mới là vô nghĩa. Do đóm một số bài học rút ra từ chính sách thuốc cùng với kết quả giám sát hiệu lực thuốc SR đang sử dụng, việc đánh giá hiệu lực thuốc ACTs mới thay thế và khắc phục nhược điểm thuốc cũ để thay đổi chính sách thuốc là cần thiết. Một số bước chính tiến hành trong nghiên cứu in vivo đánh giá ACTs hiện đang tiến hành nhằm đánh giá hiệu lực, tính dung nạp và an toàn của thuốc sẽ góp phần bổ sung dữ liệu bản đồ kháng thuốc tại Việt Nam cũng như góp phần thay đổi chính sách thuốc theo từng giai đoạn. Do vậy, nghiên cứu tiến hành nhằm Đánh giá hiệu lực thuốc phối hợp dihydroartemisinin plus piperaquine trong điều trị sốt rét do P. falciparum chưa biến chứng.
Đối tượng và phương pháp nghiên cứu
Nghiên cứu được tiến hành từ tháng 5/2011-5/2012 tại xã IaKe, huyện Phú Thiện, tỉnh Gia Lai với thiết kế nghiên cứu là thử nghiệm lâm sàng không ngẫu nhiên, tự chứng theo đề cương chuẩn của Tổ chức Y tế thế giới và Mạng lưới kháng thuốc toàn cầu (2009). Trong nghiên cứu này, tỷ lệ thất bại thuốc phối hợp DHA-PPQ theo một nghiên cứu trước đây là 20%, thì tỷ lệ thất bại lâm sàng quần thể ước tính là p (20%), CI: 95%, độ chính xác (d): 10%. Khi đó cỡ mẫu tối thiểu cần nghiên cứu đánh giá: n = 61 bệnh nhân.
Tiêu chuẩn chọn bệnh và loại trừ: Tiêu chuẩn chọn bệnh tuổi từ 6 tháng tuổi trở lên đến dưới 70 tuổi; nhiễm đơn thuần loại KSTSR P. falciparum; mật độ KSTSR thể vô tính P. falciparum trong máu từ 1.000-100.000/µl máu; nhiệt độ nách hoặc tai ≥ 37.5 °C hoặc nhiệt độ dưới lưỡi/ đại tràng ≥ 38 °C; chưa dùng một loại thuốc SR nào (kiểm tra qua thử nước tiểu các phụ nữ trong độ tuổi sinh đẻ); bệnh nhân, hoặc người thân, hoặc giám hộ đồng ý hợp tác nghiên cứu. Tiêu chuẩn loại trừ: nhỏ hơn 6 tháng tuổi hoặc lớn hơn 70 tuổi; phụ nữ đang có thai, hoặc đang cho con bú; người đang có bệnh rối loạn tâm thần kinh, động kinh; nôn mửa, tiêu chảy trầm trọng hoặc thể trạng không hấp thu được thuốc; sốt rét có biến chứng hoặc mắc các bệnh nhiễm trùng phối hợp; nhiễm sốt rét phối hợp P. falciparum + P. vivax hoặc loài khác; bệnh nhân đã dùng TSR hoặc kháng sinh có hoạt tính TSR trong 48 giờ trước khi tham gia nghiên cứu.
Phân tích và xử lý số liệu: kết quả nghiên cứu thu thập được tổng hợp, phân tích và xử lý theo phần mềm in vivo phiên bản 7.1 Pascal Ringwald, WHO (2009); đánh giá về mặt gen học: Phân tích PCR để phân biệt giữa tái phát và tái nhiễm, phân tích kiểu gen dựa trên đa dạng di truyền kiểu gen SMP1, SMP2 và GLURP (msp1, msp2 và glurp). Phân tích số lượng và tỷ lệtrong kết quả có hiệu chỉnh PCR và chưa hiệu chỉnh PCR với độ tin cậy 95% qua theo dõi đến 42 ngày (thất bại điều trị sớm, thất bại điều trị muộn, thất bại lâm sàng muộn, thất bại ký sinh trùng muộn, đáp ứng lâm sàng và ký sinh trùng đầy đủ).Thời gian sạch KSTSR (được định nghĩa là khoảng thời gian tính bằng giờ kể từ liều điều trị đầu tiên cho đến khi xét nghiệm có 3 lam máu liên tiếp âm tính với P. falciparum hay P. vivax).
Đánh giá về mặt hiệu lực theo Tổ chức Y tế thế giới (2009)
Phân loại kết quả về hiệu lực thuốc (WHO, 2009)
Phân loại đánh giá hiệu quả điều trị theo tiêu chuẩn TCYTTG (2009) | |
Thất bại điều trị sớm (ETF_Early Treatment Failure) | |
-Xuất hiện các dấu chứng của sốt rét nguy hiểm hoặc nghiêm trọng vào ngày D1, xuất hiện D2hoặcD3, kèm có mặt KSTSR trong máu; -KSTSR vào ngày D2 cao hơn D0 bất kể thân nhiệt; -Xuất hiện KSTSR trong máu vào ngày D3 đi kèm thân nhiệt ≥ 37.5ºC; -KSTSR trong máu vào ngày D3 ≥ 25% so với MĐKSTSR ngày D0. | |
Thất bại điều trị muộn (LTF_Late Treatment Failure), chia làm hai loại: | |
Thất bại lâm sàng muộn (LCF_Late Clinical Failure) -Xuất hiện các dấu chứng sốt rét nặng và nguy hiểm vào bất kỳ ngày nào từ D4 đến D42 với sự có mặt của KSTSR trong máu, không có tiêu chuẩn nào của ETF trước đó; -Có mặt KSTSR trong máu và thân nhiệt ≥ 37.5ºC hoặc có tiền sử sốt trong vùng sốt rét lan truyền thấp đến trung bình ở bất kỳ ngày nào từ D4 đến D42, không có bất kỳ dấu hiệu nào của ETF trước đó; Thất bại ký sinh trùng muộn (LPF_Late Parasitological Failure) -Có mặt KSTSR trong máu vào bất kỳ ngày nào từ D7 đến D42 và thân nhiệt < 37.5ºC, không có bất kỳ tiêu chuẩn nào của ETF và LCF trước đó. | |
|
Đáp ứng lâm sàng, KST đầy đủ (ACPR_Adequate Clinical and Parasitological Response) - Không có xuất hiện KSTSR trong máu vào D42, bất luận nhiệt độ nách thế nào và không có bất kỳ tiêu chuẩn nào của ETF, LCF và LPF trước đó. | |
Kết quả
Hiệu lực dihydroartemisinine + piperaquine (DHA-PPQ) trong điều trị P. falciparum
Hiệu lực thuốc DHA-PPQ trong điều trị P. falciparum trước và sau hiệu chỉnh PCR
Chỉ số đánh giá về hiệu lực | Trước hiệu chỉnh PCR (n = 65) | Sau hiệu chỉnh PCR (n = 65) |
SL | % | SL | % |
Hiệu lực | ETF | 2 | 3,71 | 2 | 3,71 |
LCF | 3 | 4,62 | 1 | 1,29 |
LPF | 0 | 0 | 0 | 0 |
ACPR | 55 | 91,67 | 57 | 95,0 |
Tổng số phân tích | 60 | | 60 | |
| Rút khỏi nghiên cứu | 0 | 0 | 0 | |
Mất theo dõi (sau D7) | 5 | 7,69 | 5 | 7,69 |
Tổng số nghiên cứu | 65 | | 65 | |
 |
| Phân biệt tái phát và tái nhiễm các ca thất bại điều trị bằng kỹ thuật PCR |
Với các kết quả thất bại lâm sàng muộn (LCF) trên điểm Gia Lai sau khi phân dựa vào PCR để đánh giá tái phát hay tái nhiễm P. falciparum, hiệu lực phác đồ được hiệu chỉnh lại cho thấy tỷ lệ ACPR tăng từ 91,67% lên ACPR » 95% và số trường hợp LCF giảm xuống từ 3 xuống còn 1 (4,62% à 1.29%) và 2 trường hợp còn lại chỉ là tái nhiễm hay nhiễm mới, 2 trường hợp thất bại điều trị sớm (ETF) vẫn giữ nguyên (3,71%).
Phân tích PCR xác định tái phát và tái nhiễm dựa in vivo và PCR
Mã BN | Mật độ KSTSR | Phân loại in vivo thời điểm Dthất bại | Phân loại sau hiệu chỉnh PCR |
Do | Dthất bại |
GLAK29 | 45.245 | 108 (P.f) | LCF (D42) | Tái nhiễm |
GLAK48 | 11.544 | 72 (P.f) | LCF (D42) | Tái nhiễm |
GLAK62 | 40.320 | 81.030 (P.f) | LCF (D26) | Tái phát (recrudesence) |
Ca thất bại lâm sàng muộn (LCF) trên in vivo được phân tích PCR cho thấy 2 ca tái nhiễm P. falciparum là 29GLAK và 48GLAK vào ngày D42. Ca 62GLAK là tái phát vào thời điểm D26.
Diễn tiến và tốc độ làm sạch ký sinh trùng từ D0 đến ≥ D3 do thuốc DHA-PPQ
Mã bệnh nhân | Diễn tiến làm sạch KSTSR P. falciparum |
STT | Code | Tuổi | D0 | D1 | D2 | D3 | D4 | D5 |
Phác đồ DHA-PPQ (Arterakine) |
1 | GLAK05 | 29 | 99.857 | 36.666 | 4.890 | 282 | 80 | 0 |
2 | GLAK14 | 32 | 48.875 | 2.130 | 165 | 48 | 0 | 0 |
3 | GLAK 15 | 30 | 75.559 | 16.395 | 360 | 6 | 0 | 0 |
4 | GLAK23 | 28 | 46.941 | 29.480 | 102 | 537 | 0 | 0 |
5 | GLAK27 | 15 | 56.303 | 6.225 | 66 | 12 | 0 | 0 |
6 | GLAK44 | 33 | 43.385 | 17.139 | 1.875 | 66 | 0 | 0 |
7 | GLAK46 | 13 | 29.919 | 17.213 | 1.695 | 162 | 0 | 0 |
8 | GLAK60 | 14 | 16.493 | 1.155 | 54 | 24 | 0 | 0 |
9 | GLAK61 | 31 | 31.014 | 11.333 | 756 | 267 | 0 | 0 |
10 | GLAK62 | 4 | 40.320 | 6.120 | 201 | 150 | Tái phát |
11 | GLAK65 | 5 | 49.673 | 12.300 | 483 | 36 | 0 | 0 |
MĐKSTSR trung bình D0/mL | 44.121 | 9.633 | 358 | 66 | 8 | 0 |
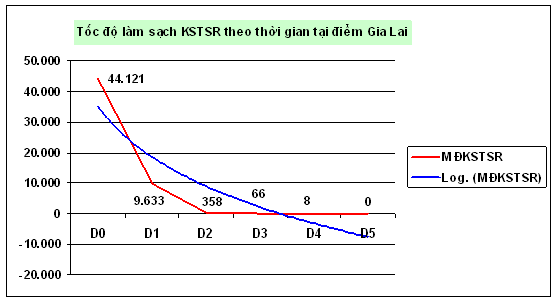 |
Diễn tiến làm sạch ký sinh trùng theo từng ngày của thuốc DHA-PPQ |
Trong số 65 ca đánh giá, có đến 11 ca (≈ 17%) còn tồn tại dương tính đến ngày D3 hoặc D4. Số liệu cho thấy diễn tiến làm sạch KSTSR trung bình qua thời gian mỗi 24 giờ từ D0 đến D3 hoặc D4 giảm rất rõ theo từ 44.121/mL à 9.633/mL à 358/mL à 66/mL à 8/mL à0/mL.
Phân tích tốc độ cắt KST P. falciparum của phác đồ DHA-PPQ
| Diễn tiến cắt KSTSR qua mỗi 12 giờ |
Mật độ KSTSR/ml ngày D0 | 32.197 (16.520-76.268) |
Thời gian sạch KST (PCT) | 61,5 (36,2-79,6) |
Sạch KST sau mỗi 12 giờ | SL(%) |
- Sau 12 giờ | 36 (55,38) |
- Sau 24 giờ | 50 (76,92) |
- Sau 36 giờ | 52 (80,0) |
- Sau 48 giờ | 54 (83,08) |
- Sau 60 giờ | 54 (83,08) |
- Sau 72 giờ | 54 (83,08) |
- Sau 84 giờ | 64(98,46) |
- Sau 96 giờ | 64(98,46) |
- Sau 108 giờ | 65(100%) |
Bảng trên cho thấy thời gian làm sạch dung khối ký sinh trùng sau mỗi 12 giờ rất nhanh, đến sau 3 ngày (72 giờ) chỉ có 83,08% số ca sạch ký sinh trùng và đến giờ thứ 108 mới sạch hoàn toàn.
Bàn luận
Mục đích chính của thử nghiệm in vivo về hiệu lực ACTs là hỗ trợ cho các kết quả dựa trên chứng cứ nhằm thay đổi chính sách thuốc tại Việt Nam. Nghiên cứu này chỉ ra thuốc DHA-PPQ hiệu lực cao và dung nạp thuốc tốt.
Tại điểm Iake, một hiện tượng có vấn đề cho thấy có sự giảm hiệu lực thuốc DHA-PPQlà 91,67% và sau khi hiệu chỉnh PCR hiệu lực thuốc thật sự tăng lên gần 95% đi kèm theo 11/65 số ca (≈ 17%) tồn tại ký sinh trùng thể vô tính trong máu ngày D3 hoặc kéo dài hơn về thời gian làm sạch ký sinh trùng như một nguy cơ cao phát triển kháng thuốc do áp lực thuốc trong vùng này. Theo định nghĩa của Chương trình sốt rét toàn cầu của Tổ chức Y tế thế giới (WHO/Global Malaria Programme) và Mạng lưới kháng thuốc sốt rét toàn cầu (World wide antimalarial drug resistance Network_WWARN) định nghĩa sự tồn tại ký sinh trùng dương tính ngày D3 như một chỉ điểm lâm sàng gián tiếp kháng thuốc (WHO., 2010). Hơn nữa, gần đây WHO đã sử dụng một định nghĩa: (i) Một sự gia tăng thời gian làm sạch ký sinh trùng khi bằng chứng có hơn 10% số ca còn tồn tại ký sinh trùng ở ngày D3 sau điều trị ACTs (nghi ngờ kháng); hoặc (ii) Một sự thất bại điều trị có bằng chứng có tồn tại ký sinh trùng ngày D3 và hoặc có tồn tại ký sinh trùng vào D7 hoặc tái phát lại sau ngày D7 trong vòng 28/42 ngày theo dõi, sau điều trị cùng với nồng độ thuốc trong máu đủ (xác định kháng). Như thế, trong phân tích này, tỷ lệ ký sinh trùng dương tính vào ngày D3 ≈ 17% > 10% , do thiếu dữ liệu phân tích về mặt dược động học nên những ca này chỉ có thể kết luận là nghi ngờ kháng thuốc.
Trường hợp thất bại điều trị sớm có liên quan đến lách bất thường (1 ca cắt lách và 1 ca teo lách bẩm sinh) nên có thể khiến cho quá trình chậm làm sạch ký sinh trùng vì lách vốn dĩ là “mồ chôn” các hồng cầu nhiễm và không nhiễm. Điều này có thể phù hợp với các nghiên cứu trước đây bởi Teuscher (2010) cho thấy sau điều trị với artesunate, các thể nhẫn của P. falciparum trở nên ngủ và khoảng 0,001–1,313% số ca hồi phục phát triển tùy thuộc vào chủng ký sinh trùng và lệ thuộc vào liều. Để xác định có hay không cùng hiện tượng này xảy ra trên in vivo, sự phục hồi thể ngủ được đánh giá qua sử dụng mô hình P. v. vinckei. Kết quả cho thấy các thể ngủ cũng phát hiện tương tự như trên in vitro có mặt trên các con chuột được điều trị và ngày để ký sinh trùng phục hồi có thể liên quan đến số lượng KST thể ngủ (dormant parasites) có mặt trong các con chuột còn sống; tuy nhiên, có thể thay đổi trên các con chuột không có lách. Dựa trên thiết kế mô hình thực nghiệm chúng ta không thể tính toán chính xác tỷ lệ phục hồi.
Trong 2 ca tái nhiễm ở ngày D42 (GLAK29 và GLAK48) và 1 ca tái phát vào ngày D26 (GLAK62). Trong sốt rét, các hồng cầu bị ký sinh nhưng thực tế không chứa KST tìm thấy trong hệ thống tuần hoàn. Điều này có thể có sự gia tăng nhờ vào sự loại do lách với các KST trong hồng cầu bị tổn thương hay bị chết và nhìn thấy phần lớn hồng cầu nguyên vẹn trong hệ tuần hoàn. Trong một nghiên cứu trên 5 bệnh nhân mắc sốt rét do P. falciparum có tiền sử cắt lách trước đó, người ta cho thấy các bệnh nhân đó đều có hồng cầu RESA-RBCs lưu hành, nhưng ngược lại không phát hiện các hồng cầu RESA-RBCs trên tất cả bệnh nhân sốt rét mà lách còn nguyên vẹn. Sự làm sạch KSTSR sau khi điều trị artesunate kéo dài đáng kể, mặc dù KST dường như đã chết không thể nuôi cấy trên ex vivo mà phát triển được. Các quan sát này xác định vai trò của lách trong việc làm sạch các hồng cầu bị ký sinh khi điều trị bằng dẫn suất artemisinins (Kesinee Chotivanich et al.,2002). Việc xác định kháng hay không kháng thì những nghiên cứu tiếp theo phải làm in vivo, in vitro, khía cạnh phân tử và dược động học để thiết lập mô hình kháng artemisinin như thế nào?
Kết luận
- Với hiệu lực DHA-PPQ hiện đang như một thuốc đầu tay và ưu tiên trong điều trị sốt rét do P. falciparum khoảng 95% và thời gian làm sạch KST nhanh, sẽ giúp làm giảm nhanh dung khối ký sinh trùng, giảm thiểu số ca sốt rét ác tính;
- Song, với tỷ lệ tồn tại KST thể vô tính ở ngày D3 cao (17%) sau điều trị DHA-PPQ cùng với tỷ lệ thất bại lâm sàng muộn như một chỉ điểm phát triển kháng thuốc cao. Do vậy, việc cần thiết là kế hoạch giám sát thường quy hiệu lực thuốc tại vùng SRLH như ở Iake, huyện Phú Thiện để sớm cảnh báo về tình trạng kháng thuốc cũng như thay đổi chính sách thuốc theo từng giai đoạn.
Tài liệu tham khảo
1.Bassat Q, et al. (2009), Dihydroartemisinin-piperaquine and artemether-lumefantrine for treating uncomplicated malaria in African children: A randomised, non-inferiority trial. PLoS one 4(11): e7871.
2.D’Alessandro U, et al. (2010), Artemisinin - based combinations for treating uncomplicated malaria in African children: the 4 ABC Trial presentation at the 59th congress of ASTMH.
3.Grande T, et al., (2007). A randomised controlled trial to assess the Dihydroartemisinin-Piperaquine for the treatment uncomplicated falciparum malaria in Peru. PLoS onE 2(10): e1101.
4.Harald Noedl, Youry Se et al., (2009), Evidence of artemisinin- resistant malaria in Western Cambodia, Volume 359:2619-2620.
5.Julien Zwang, Elizabeth A. Ashley, Corine Karema et al., (2008), Safety and efficacy of Dihydroartemisinin-Piperaquine in falciparum malaria: A prospective multi - centre individual patient data analysis. PLoS Hub for Clinical Trials
6.Michelle Wykes (2011), Malaria parasite hiden in spleen. http://www.indianexpress.com/news/ malaria-parasites-hide-in-spleen
7.T.N.Trung, H.H.Quang, David T.M.E et al., (2001), Treatment of falciparum malaria in Vietnamese children: the need for combination therapy and optimised dosage regimes”. Anals. of paediatrics tropical medicine, University of Western Australia, p 2-7.
8.T.N Trung, H.H Quang, Li Guoqiao et al., (2008), Assessment of ACTs (Artemisinine based Combination Therapy) antimalarial drugs efficacy for the treatment of uncomplicated falciparum malaria in hyperendemic sites, Central and West-highland area, Vietnam (2004-2008). Journal of medicine of Ho Chi Minh, Vol.12-supplement of No.4: 28-34.
9.Valecha N, et al., (2010), An Open-Label, Randomised Study of Dihydroartemisinin-Piperaquine Versus artesunate+mefloquine for falciparum malaria in Asia. PLoS onE 5(7): e11880.
10.WHO (2010), Global report antimalarial drugs efficacy and drugs resistance 2000-2010