(Tiếp theo Phần 2)
VẬT LIỆU VÀ PHƯƠNG PHÁP
Mục tiêu chính là phát triển và triển khai một mô hình dựa trên AI mạnh mẽ để chẩn đoán chính xác bệnh sốt rét bằng cách sử dụng các hình ảnh phết máu soi dưới KHV. Phương pháp luận được đề xuất được thiết kế theo một cách tiếp cận đa giai đoạn, trong đó mỗi giai đoạn góp phần vào độ chính xác và độ tin cậy của quy trình chẩn đoán. Quy trình làm việc toàn diện, như được minh họa trong Hình 1, bao gồm nhiều giai đoạn khác nhau trong việc phát triển và triển khai mô hình, bao gồm tiền xử lý dữ liệu, trích xuất đặc trưng, huấn luyện, kiểm định và thử nghiệm mô hình.
Quy trình có cấu trúc này nhằm đảm bảo độ chính xác và hiệu quả chẩn đoán cao, giải quyết nhu cầu cấp thiết về việc phát hiện bệnh sốt rét một cách hiệu quả trong các môi trường lâm sàng và thực địa.
Hình. 1. Quy trình minh họa đề xuất để chẩn đoán bệnh sốt rét minh họa cho (a) Mô hình học sâu (DL) đầu cuối, (b)Thuật toán áp dụng để trích xuất đặc trưng và (c)Thuật toán được áp dụng để phân loại.
1. Bộ dữ liệu
Bộ dữ liệu “Cell Images for Detecting Malaria”²¹, được lưu trữ trên Kaggle là một bộ sưu tập được tuyển chọn kỹ lưỡng gồm các hình ảnh phết máu soi dưới KHV, được thiết kế để tạo điều kiện thuận lợi cho nghiên cứu và phát triển trong việc phát hiện bệnh sốt rét bằng các mô hình học máy và học sâu. Bộ dữ liệu này bao gồm 27.558 hình ảnh, được chia đều thành hai loại: Nhiễm ký sinh trùng (tế bào nhiễm sốt rét) và Không nhiễm KSTSR (tế bào khỏe mạnh). Các hình ảnh được chụp bằng KHV quang học ở độ phóng đại 100x, đảm bảo độ rõ nét hình ảnh cao, lý tưởng cho các ứng dụng học máy và học sâu. Hình ảnh đầu vào ban đầu có kích thước 150×150. Bộ dữ liệu đã trải qua một số bước tiền xử lý, chẳng hạn như thay đổi kích thước để phù hợp với lớp đầu vào của mô hình AI được đề xuất.
Bộ dữ liệu được tổ chức một cách có hệ thống thành hai thư mục: Thư mục Nhiễm ký sinh trùng chứa các hình ảnh tế bào hồng cầu bị nhiễm kKSTSR Plasmodium spp., được đánh dấu bởi các đặc điểm hình ảnh rõ rệt như hình dạng bất thường, các đốm đen và cấu trúc bên trong không đồng đều. Thư mục Không nhiễm bao gồm các hình ảnh tế bào hồng cầu khỏe mạnh, đặc trưng bởi cấu trúc mịn, hình dạng đồng nhất và không có các cấu trúc, tạp chất của ký sinh trùng. Cấu trúc này giúp đơn giản hóa các tác vụ tải và tiền xử lý dữ liệu cho các nhà nghiên cứu và nhà phát triển.
Một trong những đặc điểm nổi bật của bộ dữ liệu này là sự phân bố cân bằng, với số lượng hình ảnh bằng nhau ở mỗi loại. Sự cân bằng này giúp giảm thiểu các vấn đề mất cân bằng lớp, đảm bảo rằng các mô hình học máy có thể huấn luyện hiệu quả mà không bị thiên vị về một lớp cụ thể nào. Ngoài ra, bộ dữ liệu còn thể hiện sự đa dạng sinh học, gồm một loạt các hình thái tế bào, các biến thể nhuộm màu và các kiểu mẫu phản ánh sự phức tạp gặp phải trong môi trường lâm sàng thực tế.
Hình. 2. Các mẫu của bộ dữ liệu được sử dụng: (a) Mẫu không nhiễm, (b) Mẫu bị nhiễm
Nhìn chung, bộ dữ liệu này là một nguồn tài nguyên vô giá để thúc đẩy các giải pháp chăm sóc sức khỏe dựa trên AI. Nó đặc biệt phù hợp để huấn luyện, kiểm định và thử nghiệm các mô hình phân loại cũng như cho học chuyển giao (transfer learning), nơi các mô hình được huấn luyện trước được tinh chỉnh cho các tác vụ phát hiện sốt rét. Các đặc điểm như chất lượng cao, tính đa dạng và được gán nhãn tốt của bộ dữ liệu này đảm bảo rằng các mô hình được huấn luyện trên đó sẽ mạnh mẽ, đáng tin cậy và có khả năng hoạt động hiệu quả trong các kịch bản chẩn đoán thực tế.
Trong quá trình triển khai mô hình AI được đề xuất, bộ dữ liệu được chia thành 70% để huấn luyện, 15% để kiểm định và 15% để thử nghiệm. Các ví dụ về bộ dữ liệu đã sử dụng được cung cấp trong Hình 2. Sự phân bố số lượng hình ảnh giữa các lớp mục tiêu được trình bày trong Bảng 2.
Bảng 2. Phân bố của bộ dữ liệu được sử dụng đánh giá nhiễm và không nhiễm KSTSR
| Phân loại | Không nhiễm KSTSR | Nhiễm KSTSR |
| Huấn luyện | 9645 | 9645 |
| Kiểm định | 2067 | 2067 |
| Kiểm tra | 2067 | 2067 |
Giai đoạn (a): Triển khai các Mô hình học sâu đầu - cuối
Trong giai đoạn này, phương pháp luận kết hợp độ mạnh của học chuyển giao (transfer learning) và các phương pháp học sâu đầu cuối để xử lý các hình ảnh phết máu soi dưới KHV nhằm chẩn đoán bệnh sốt rét. Ba kiến trúc Mạng nơ-ron tích chập (CNN) tiên tiến, ResNet-50²², VGG-16²³ và DenseNet-201²⁴ được sử dụng làm bộ trích xuất đặc trưng. Các mô hình này sử dụng các trọng số đã được huấn luyện trước từ các bộ dữ liệu quy mô lớn, cho phép chúng nhận dạng các mẫu phức tạp trong hình ảnh tế bào máu. Trong các mô hình này đã thực hiện học chuyển giao bằng cách huấn luyện lại phần đầu cuối của CNN, bao gồm một lớp kết nối đầy đủ, một lớp dropout, một lớp SoftMax và một lớp phân loại. Mỗi mô hình được đề xuất đều giữ lại các tham số chính trong lớp tích chập, bao gồm số lượng bộ lọc, độ dài bước nhảy (stride length) và các trọng số của nó.
Đối với ResNet-50, mô hình này thu được 2048 đặc trưng phân cấp sâu thông qua các kết nối dư, giải quyết các vấn đề tiêu biến đạo hàm (vanishing gradient) để việc học đạt hiệu quả. Trong khi đó, VGG-16 xác định 4096 đặc trưng không gian bằng cách sử dụng kiến trúc tích chập đồng nhất, đảm bảo việc trích xuất các chi tiết hình ảnh một cách nhất quán. Ngoài ra, DenseNet-201 tăng cường sự lan truyền đặc trưng bằng cách tạo ra các lớp kết nối dày đặc, cải thiện sự phong phú và mức độ liên quan của 1920 đặc trưng được trích xuất.Ngoài việc trích xuất đặc trưng, các kiến trúc này còn được huấn luyện như các mô hình đầu cuối. Điều này cho phép toàn bộ mạng từ lớp đầu vào đến lớp phân loại, được tinh chỉnh đặc biệt cho việc chẩn đoán bệnh sốt rét. Bằng cách điều chỉnh các mô hình đã được huấn luyện trước cho tác vụ cụ thể, các mạng này học cách tối ưu hóa cả các đặc trưng cấp thấp và cấp cao liên quan đến việc xác định tế bào bị nhiễm và tế bào khỏe mạnh. Cách tiếp cận kép này không chỉ khai thác các thế mạnh của học chuyển giao mà còn tận dụng khả năng thích ứng của các mô hình học sâu, tạo ra một nền tảng vững chắc để chẩn đoán bệnh sốt rét một cách chính xác.
Trong giai đoạn này, phương pháp luận kết hợp các thế mạnh của học chuyển giao và các phương pháp học sâu đầu cuối để xử lý các hình ảnh phết máu soi dưới kính hiển vi nhằm chẩn đoán bệnh sốt rét. Ba kiến trúc mạng nơ-ron tích chập (CNN) tiên tiến - ResNet-50, VGG-16 và DenseNet-201, đóng vai trò là trụ cột cho việc trích xuất đặc trưng và phân loại. Các mô hình này tận dụng các trọng số đã được huấn luyện trước từ các bộ dữ liệu quy mô lớn như ImageNet, cho phép chúng phát hiện các mẫu phức tạp và tinh vi trong hình ảnh tế bào máu với độ chính xác và hiệu quả vượt trội. Quá trình trích xuất đặc trưng từ các mô hình CNN có thể được biểu diễn về mặt toán học như trong Phương trình (1).
Trong đó X là hình ảnh đầu vào,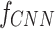 biểu thị hàm trích xuất đặc trưng của mô hình CNN,
biểu thị hàm trích xuất đặc trưng của mô hình CNN, 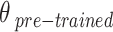 là các trọng số được huấn luyện trước, F là vector đặc trưng kết quả.
là các trọng số được huấn luyện trước, F là vector đặc trưng kết quả.
Mỗi kiến trúc đóng góp một cách riêng biệt vào việc trích xuất đặc trưng. ResNet-50 thu được 2048 đặc trưng phân cấp sâu thông qua khung học tồn lưu (residual learning), vốn giới thiệu kết nối tắt (shortcut connections) để bỏ qua các lớp. Kết nối dư này có thể được mô tả như trong Phương trình (2).
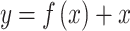 | 2 |
Trong đó x là đầu vào cho khối tồn dư, f(x) là phép biến đổi đã học được, y là đầu ra của khối tồn dư. VGG-16, nổi tiếng với cấu trúc đơn giản và tuần tự, trích xuất 4096 đặc trưng không gian bằng cách dùng các lớp tích chập đồng nhất với bộ lọc nhỏ (3x3). Phương trình (3) trình bày đầu ra của lớp này.
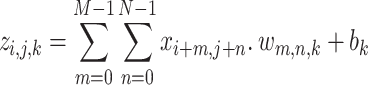 | 3 |
Trong đó
là bản đồ đặc trưng đầu ra, 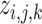 là bản đồ đặc trưng đầu vào,
là bản đồ đặc trưng đầu vào,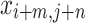 là các trọng số của bộ lọc,
là các trọng số của bộ lọc, 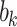 là số hạng thiên vị (bias), và M và N là các chiều của bộ lọc. Cách tiếp cận này đảm bảo phát hiện chính xác các đặc điểm không gian như hình thái và cấu trúc tế bào. DenseNet-201 tăng cường sự lan truyền và tái sử dụng đặc trưng thông qua các lớp được kết nối dày đặc, nơi mỗi lớp được kết nối với tất cả các lớp trước đó. Điều này có thể được biểu diễn như trong Phương trình (4).
là số hạng thiên vị (bias), và M và N là các chiều của bộ lọc. Cách tiếp cận này đảm bảo phát hiện chính xác các đặc điểm không gian như hình thái và cấu trúc tế bào. DenseNet-201 tăng cường sự lan truyền và tái sử dụng đặc trưng thông qua các lớp được kết nối dày đặc, nơi mỗi lớp được kết nối với tất cả các lớp trước đó. Điều này có thể được biểu diễn như trong Phương trình (4).
Trong đó 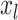 là đầu ra của lớp thứ
là đầu ra của lớp thứ 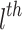 ,
, 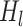 là phép biến đổi đã học được, và
là phép biến đổi đã học được, và 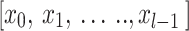 biểu thị sự ghép nối (concatenation) của các bản đồ đặc trưng từ các lớp trước đó. Kết nối này giúp trích xuất 1920 đặc trưng có độ liên quan cao, góp phần tạo nên một tập hợp đặc trưng phong phú.Ngoài việc trích xuất đặc trưng, các kiến trúc CNN này còn được tinh chỉnh như các mô hình học sâu đầu cuối. Việc tinh chỉnh sẽ tối ưu hóa các tham số
biểu thị sự ghép nối (concatenation) của các bản đồ đặc trưng từ các lớp trước đó. Kết nối này giúp trích xuất 1920 đặc trưng có độ liên quan cao, góp phần tạo nên một tập hợp đặc trưng phong phú.Ngoài việc trích xuất đặc trưng, các kiến trúc CNN này còn được tinh chỉnh như các mô hình học sâu đầu cuối. Việc tinh chỉnh sẽ tối ưu hóa các tham số 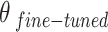 cho tác vụ cụ thể là chẩn đoán bệnh sốt rét bằng cách giảm thiểu một hàm tổn thất như trong Phương trình (5).
cho tác vụ cụ thể là chẩn đoán bệnh sốt rét bằng cách giảm thiểu một hàm tổn thất như trong Phương trình (5).
Trong đó 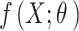 là đầu ra dự đoán của mô hình, y là nhãn thực tế (ground truth) và L là hàm tổn thất entropy chéo (cross-entropy).
là đầu ra dự đoán của mô hình, y là nhãn thực tế (ground truth) và L là hàm tổn thất entropy chéo (cross-entropy).
Quá trình này đảm bảo rằng các mô hình học được cả các đặc trưng cấp thấp (như cấu trúc và hình dạng) và các đặc trưng cấp cao (như các mẫu KSTSR) đặc thù của việc soi phết máu dưới kHV.
Để biết thêm thông tin, Bảng 3 tóm tắt các siêu tham số huấn luyện được sử dụng cho việc huấn luyện các mô hình được đề xuất, phản ánh một cấu hình được tinh chỉnh cẩn thận nhằm cân bằng giữa sự ổn định trong học, hiệu quả và khả năng tổng quát hóa thông qua việc tối ưu hóa theo lô nhỏ (mini-batch), lập lịch tốc độ học (learning rate) và kiểm định định kỳ. Vì việc lựa chọn các siêu tham số huấn luyện có thể ảnh hưởng trực tiếp đến các mô hình được đề xuất²⁵.
Hơn nữa, Hình 3 cung cấp một lưu đồ của thuật toán được đề xuất, bao gồm các giai đoạn huấn luyện và thử nghiệm.
Bảng 3. Các siêu tham số huấn luyện khác nhau cho các mô hình CNN được đề xuất.
| Siêu tham số | Giá trị | Mô tả mô hình |
| Trình tối ưu hóa | SGDM | Dốc gradient ngẫu nhiên có đà (stochastic gradient descent with momentum) |
| Môi trường thực thi | Song song | Sử dụng nhiều lõi CPU/GPU để tính toán nhanh hơn |
| Kích thước lô mini | 64 | Số lượng mẫu được xử lý trong mỗi lần lặp huấn luyện |
| Số epoch tối đa | 30 | Số lần duyệt qua toàn bộ bộ dữ liệu huấn luyện |
| Hàm kích hoạt | ReLU | Bổ sung tính phi tuyến và giúp tăng tốc độ hội tụ bằng cách cho phép các mô hình học các mẫu phức tạp một cách hiệu quả |
| Tốc độ học ban đầu | 1.00E-05 | Giá trị khởi đầu của tốc độ học |
| Lịch trình tốc độ học | từng phần | Tốc độ học được điều chỉnh tại các khoảng thời gian được xác định trước |
| Tần suất kiểm định | 50 | Việc kiểm định được thực hiện sau mỗi 50 lần lặp |
Hình 3. Lưu đồ của phương pháp được đề xuất để phát hiện bệnh sốt rét.
Giai đoạn (b): Hợp nhất Đặc trưng và Giảm chiều dữ liệu
Sau khi trích xuất đặc trưng một cách độc lập bằng ResNet-50, VGG-16, và DenseNet-201, bước tiếp theo trong phương pháp luận là hợp nhất đặc trưng. Quá trình này kết hợp các bộ đặc trưng đa dạng do các mô hình này tạo ra thành một vector đặc trưng thống nhất, toàn diện. Phép toán hợp nhất được thực hiện thông qua việc ghép nối, nhằm tổng hợp các vector đặc trưng từ ba mô hình theo Phương trình (6).
Trong đó 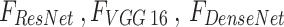 lần lượt là các vector đặc trưng được trích xuất từ ResNet-50, VGG-16, và DenseNet-201,
lần lượt là các vector đặc trưng được trích xuất từ ResNet-50, VGG-16, và DenseNet-201, 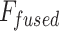 biểu thị vector đặc trưng đã được hợp nhất. Tổng số đặc trưng sau khi ghép nối là 8064.
biểu thị vector đặc trưng đã được hợp nhất. Tổng số đặc trưng sau khi ghép nối là 8064.
Vector đặc trưng đã được hợp nhất này cung cấp một biểu diễn phong phú hơn bằng cách kết hợp cả các mẫu toàn cục (thu được bởi ResNet-50) và các chi tiết không gian cục bộ (thu được bởi VGG-16 và DenseNet-201). Mặc dù các đặc trưng kết hợp giúp tăng cường đáng kể khả năng phân biệt giữa tế bào nhiễm sốt rét và tế bào khỏe mạnh của mô hình, chiều dữ liệu cao của chúng lại gây ra những thách thức về độ phức tạp tính toán và hiện tượng quá khớp (overfitting).
Để giải quyết những thách thức này, Phân tích Thành phần Chính (Principal Component Analysis - PCA) được sử dụng để giảm chiều dữ liệu. PCA biến đổi vector đặc trưng đã hợp nhất có chiều dữ liệu cao thành một không gian có chiều dữ liệu thấp hơn bằng cách tìm ra các thành phần chính thu được phương sai tối đa trong dữ liệu. Phép biến đổi có thể được biểu diễn như trong Phương trình (7).
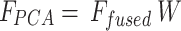
7
Trong đó là Ffused ma trận đặc trưng đã hợp nhất ban đầu có kích thước Nx8064, với N là số lượng mẫu. Ma trận chiếu W được tính toán bằng cách giải bài toán phân rã trị riêng (eigenvalue decomposition) của ma trận hiệp phương sai của Ffused .
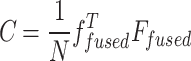
8
Phương trình 8 giới thiệu ma trận hiệp phương sai (C) của ma trận đặc trưng đã hợp nhất. Đây là một ma trận vuông ghi lại các mối quan hệ giữa các đặc trưng trong không gian đặc trưng đã hợp nhất. Bằng cách chỉ chọn k thành phần chính hàng đầu thu được 95% phương sai, PCA đảm bảo rằng các đặc trưng có tính phân biệt cao nhất được bảo toàn trong khi giảm không gian đặc trưng. Việc giảm chiều này giúp giảm thiểu độ phức tạp tính toán, hạn chế hiện tượng quá khớp, và tăng tốc các tác vụ phân loại tiếp theo, đồng thời vẫn duy trì độ chính xác chẩn đoán cao.
- 4.Giai đoạn (c): Khung phân loại hỗn hợp
Sau khi giảm chiều dữ liệu, vector đặc trưng đã được tinh chỉnh sẽ được xử lý thông qua một khung phân loại hỗn hợp, kết hợp các thế mạnh của các mô hình học máy truyền thống và học sâu. Khung này bao gồm hai thành phần: Máy vector hỗ trợ (Support Vector Machine - SVM) và Mạng bộ nhớ dài-ngắn (Long Short-Term Memory Networks - LSTM). Mỗi thành phần đóng một vai trò quan trọng trong việc đảm bảo phân loại mạnh mẽ và chính xác, bổ sung cho năng lực của nhau.
- Máy vector Hỗ trợ (SVM)
SVM là một thuật toán học có giám sát mạnh mẽ, vượt trội trong việc xác định các ranh giới quyết định tối ưu giữa các lớp, ngay cả trong các không gian nhiều chiều²⁶. Trong khung này, vector đặc trưng đã được giảm chiều được cung cấp làm đầu vào cho bộ phân loại SVM, hoạt động bằng cách tìm một siêu phẳng (hyperplane) có thể phân tách tối đa hai lớp: mẫu nhiễm sốt rét và mẫu khỏe mạnh. Bộ phân loại SVM nhằm mục đích tối đa hóa lề (margin), là khoảng cách giữa siêu phẳng và các điểm dữ liệu gần nhất ở mỗi bên, được gọi là các vector hỗ trợ. Cách tiếp cận này đảm bảo rằng bộ phân loại có khả năng tổng quát hóa tốt trên dữ liệu chưa thấy, làm cho nó đặc biệt hiệu quả cho các tác vụ phân loại nhị phân như chẩn đoán sốt rét. Tính mạnh mẽ và độ tin cậy của SVM làm cho nó trở thành một thành phần thiết yếu của khung hỗn hợp này. Mục tiêu cốt lõi của SVM là tối đa hóa lề giữa siêu phẳng phân tách và các điểm dữ liệu gần nhất của mỗi lớp, được gọi là các vector hỗ trợ. Siêu phẳng tối ưu có thể được biểu diễn về mặt toán học trong các Phương trình (9–11)
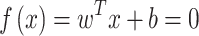
9
Trong đó x là vector đặc trưng đầu vào, w là vector trọng số trực giao với siêu phẳng, b là số hạng thiên vị.Để tìm siêu phẳng tối ưu, SVM giải bài toán tối ưu lồi sau:
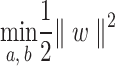
10
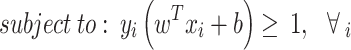
11
Trong đó 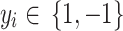 là các nhãn lớp, xi là các mẫu huấn luyện.
là các nhãn lớp, xi là các mẫu huấn luyện.
Bằng cách tối đa hóa lề 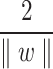 , SVM giảm thiểu hiện tượng quá khớp và cải thiện hiệu suất tổng quát hóa trên dữ liệu thử nghiệm chưa thấy. Đối với dữ liệu không thể phân tách tuyến tính, SVM tích hợp các hàm hạt nhân
, SVM giảm thiểu hiện tượng quá khớp và cải thiện hiệu suất tổng quát hóa trên dữ liệu thử nghiệm chưa thấy. Đối với dữ liệu không thể phân tách tuyến tính, SVM tích hợp các hàm hạt nhân 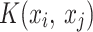 để ánh xạ dữ liệu vào một không gian có chiều cao hơn, nơi việc phân tách tuyến tính trở nên khả thi. Trong bối cảnh của nghiên cứu này, bộ phân loại SVM xử lý tập đặc trưng PCA đã được biến đổi để học siêu phẳng phân tách tốt nhất giữa các tế bào bị nhiễm và không bị nhiễm. Tính chặt chẽ về mặt toán học, diễn giải hình học, và khả năng tổng quát hóa làm cho SVM trở thành một thành phần không thể thiếu của hệ thống phân loại hỗn hợp được đề xuất.
để ánh xạ dữ liệu vào một không gian có chiều cao hơn, nơi việc phân tách tuyến tính trở nên khả thi. Trong bối cảnh của nghiên cứu này, bộ phân loại SVM xử lý tập đặc trưng PCA đã được biến đổi để học siêu phẳng phân tách tốt nhất giữa các tế bào bị nhiễm và không bị nhiễm. Tính chặt chẽ về mặt toán học, diễn giải hình học, và khả năng tổng quát hóa làm cho SVM trở thành một thành phần không thể thiếu của hệ thống phân loại hỗn hợp được đề xuất.
- b.Mạng Bộ nhớ Dài-ngắn (LSTM)
LSTM, một loại mạng nơ-ron hồi quy (recurrent neural network - RNN), được sử dụng trong khung này để nắm bắt các hình mẫu và các mối quan hệ theo ngữ cảnh trong dữ liệu. Mặc dù bản thân vector đặc trưng không mang tính tuần tự, các mạng LSTM lại vượt trội trong việc mô hình hóa các sự phụ thuộc giữa các đặc trưng, cho phép hệ thống nhận dạng các hình mẫu phức tạp biểu thị các tế bào nhiễm sốt rét¹²,¹⁹. LSTM được thiết kế với các cơ chế chuyên biệt, chẳng hạn như các cổng điều tiết luồng thông tin, đảm bảo mô hình chỉ giữ lại các mẫu phù hợp nhất và loại bỏ các chi tiết không cần thiết. Điều này làm cho LSTM đặc biệt thành thạo trong việc học các biểu diễn phức tạp và tinh vi từ dữ liệu, thêm một lớp diễn giải và tính mạnh mẽ cho quá trình phân loại. Trong bối cảnh chẩn đoán sốt rét, LSTM thêm một lớp diễn giải có khả năng nắm bắt các tương tác đặc trưng phức tạp mà có thể không thể phân tách tuyến tính²⁷.
LSTM đạt được điều này thông qua một kiến trúc tế bào nhớ có cổng, bao gồm cổng quên, cổng vào, cập nhật trạng thái tế bào, và cổng ra. Các cổng này kiểm soát luồng thông tin, lựa chọn nhớ hoặc quên các phần của đầu vào và các trạng thái ẩn trước đó, do đó cho phép mạng tập trung vào các mẫu thông tin hữu ích nhất trong khi loại bỏ những mẫu không liên quan. Các hoạt động bên trong của một tế bào LSTM tại bước thời gian t được mô tả bằng các Phương trình (12–17) sau:
- Cổng quên (Forgot gate).
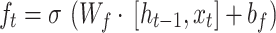
12
- Input gate. Cổng vào (Input gate).
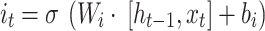
13
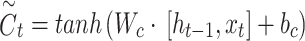
14
- Cell state update. Cập nhật trạng thái tế bào (Cell state update).
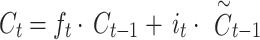
15
- Output gate. Cổng ra (Output gate).
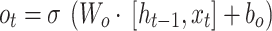
16
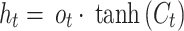
17
Trong đó xt là đầu vào tại bước thời gian t, 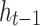 là trạng thái ẩn trước đó, Ct là trạng thái tế bào hiện tại,
là trạng thái ẩn trước đó, Ct là trạng thái tế bào hiện tại, 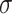 là hàm kích hoạt sigmoid, Wandb là các trọng số và số hạng thiên vị có thể huấn luyện được, tand là hàm kích hoạt tang hyperbol. Các cơ chế này cho phép LSTM giữ lại các phụ thuộc dài hạn và lọc bỏ nhiễu, điều này rất quan trọng khi học từ các mẫu sinh học phức tạp như các biến thể trong hình thái tế bào hồng cầu ở bệnh sốt rét.
là hàm kích hoạt sigmoid, Wandb là các trọng số và số hạng thiên vị có thể huấn luyện được, tand là hàm kích hoạt tang hyperbol. Các cơ chế này cho phép LSTM giữ lại các phụ thuộc dài hạn và lọc bỏ nhiễu, điều này rất quan trọng khi học từ các mẫu sinh học phức tạp như các biến thể trong hình thái tế bào hồng cầu ở bệnh sốt rét.
Hình 4.Cấu trúc của mô hình RNN (LSTM) được đề xuất để phát hiện bệnh sốt rét.
Kiến trúc RNN được thiết kế tích hợp một cấu trúc học sâu dựa trên LSTM, được tùy chỉnh để phân loại các mẫu bệnh phẩm nhiễm sốt rét so với các mẫu không nhiễm bằng cách sử dụng tập đặc trưng đã được giảm chiều thu được từ PCA. Mạng bắt đầu với một lớp đầu vào chuỗi được cấu hình cho chiều đầu vào là 3135 đặc trưng, đại diện cho các thành phần chính được suy ra từ vector đặc trưng đã hợp nhất có chiều dữ liệu cao ban đầu. Tiếp theo là một lớp LSTM với 128 đơn vị ẩn, cho phép mạng nắm bắt các phụ thuộc theo thời gian hoặc theo ngữ cảnh giữa các đặc trưng đầu vào, mặc dù chúng không phải là dữ liệu chuỗi thời gian theo nghĩa cổ điển.
Sau lớp LSTM là một lớp kết nối đầy đủ, ánh xạ các biểu diễn đặc trưng đã học được tới số lượng lớp đầu ra mong muốn (trong trường hợp này là hai). Một lớp SoftMax theo sau, chuyển đổi các điểm số thô của lớp thành các xác suất được chuẩn hóa, cho phép diễn giải các kết quả phân loại theo xác suất. Cuối cùng, lớp phân loại tính toán tổn thất trong quá trình huấn luyện và đánh giá hiệu suất dự đoán của mô hình. Kiến trúc này tận dụng hiệu quả khả năng của LSTM trong việc mô hình hóa các mối quan hệ phức tạp giữa các đặc trưng, cải thiện khả năng của hệ thống trong việc phân biệt giữa các mẫu máu nhiễm và không nhiễm sốt rét. Hình 4 mô tả cấu trúc chi tiết của mạng được đề xuất.
Để cải thiện hơn nữa độ tin cậy và độ chính xác của quy trình phân loại, phương pháp luận này tích hợp một cơ chế biểu quyết theo đa số. Cơ chế này được sử dụng để tổng hợp các dự đoán từ nhiều bộ phân loại, bao gồm ba mô hình học sâu từ đầu đến cuối (ResNet-50, VGG-16 và DenseNet-201), cũng như các bộ phân loại SVM và LSTM. Bằng cách kết hợp kết quả đầu ra của các mô hình đa dạng này, cơ chế biểu quyết theo đa số đảm bảo một quyết định dựa trên sự đồng thuận, làm giảm khả năng xảy ra sai sót phát sinh từ những hạn chế của bất kỳ mô hình đơn lẻ nào²⁸.Trong quy trình biểu quyết theo đa số, mỗi bộ phân loại sẽ dự đoán một cách độc lập xem hình ảnh phết máu đầu vào tương ứng với mẫu nhiễm sốt rét hay không nhiễm. Những dự đoán này được xem như các phiếu bầu, với mỗi mô hình đóng góp một phiếu cho quyết định cuối cùng. Nhãn lớp có đa số phiếu bầu sẽ được chọn làm kết quả phân loại cuối cùng. Ví dụ, nếu năm mô hình đưa ra các dự đoán như sau:
- ResNet-50: Nhiễm sốt rét.
- VGG-16: Nhiễm sốt rét.
- DenseNet-201: Không nhiễm.
- SVM: Nhiễm sốt rét.
- LSTM: Không nhiễm.
Do đó, lớp chiếm đa số (trong trường hợp này là Nhiễm sốt rét) được chọn làm quyết định cuối cùng.Cách tiếp cận này đặc biệt hiệu quả trong việc tận dụng các thế mạnh bổ sung cho nhau của các mô hình tham gia. Các mô hình học sâu cung cấp khả năng trích xuất đặc trưng và nhận dạng mẫu mạnh mẽ, trong khi SVM đóng góp vào việc tối ưu hóa ranh giới quyết định một cách chính xác và LSTM nắm bắt các mối quan hệ phức tạp trong dữ liệu. Bằng cách tổng hợp những góc nhìn đa dạng này, cơ chế biểu quyết theo đa số giúp giảm thiểu ảnh hưởng của các dự đoán ngoại lai và cải thiện tính mạnh mẽ tổng thể của việc phân loại.
Hơn nữa, cơ chế biểu quyết theo đa số vốn có tính thích ứng và khả năng mở rộng. Các bộ phân loại bổ sung có thể được tích hợp vào quy trình biểu quyết mà không cần thay đổi đáng kể hệ thống, qua đó nâng cao hơn nữa tính linh hoạt của nó. Cơ chế này cũng làm giảm tác động của dữ liệu nhiễu hoặc các thiên kiến riêng của mô hình, vì quyết định cuối cùng phản ánh sự đồng thuận thay vì dựa vào kết quả đầu ra của một bộ phân loại duy nhất. Kết quả của quy trình biểu quyết theo đa số cung cấp kết quả phân loại cuối cùng, xác định một cách đáng tin cậy xem hình ảnh phết máu đầu vào có nhiễm sốt rét hay không. Chiến lược dựa trên sự đồng thuận này đảm bảo rằng hệ thống chẩn đoán mang lại độ chính xác và độ tin cậy cao, phù hợp cho các ứng dụng lâm sàng trong thực tế, nơi mà độ tin cậy là yếu tố cực kỳ quan trọng.
(Còn nữa) --> Tiếp theo Phần 4
CN. Nguyễn Thái Hoàng & TS.BS. Huỳnh Hồng Quang
Viện Sốt rét-KST-CT Quy Nhơn